Immer mehr Menschen leiden an chronischen Nierenerkrankungen (chronic kidney disease, CKD). Mehr als zehn Prozent der Bevölkerung hierzulande – rund 8.3 Mio. Menschen – sind von CKD betroffen. Die eingeschränkte Nierenfunktion führt bei vielen Patient:innen zu einer Blutarmut. Ursache dieser renalen Anämie ist eine verringerte Produktion des Hormons Erythropoietin (Epo), das für die Bildung von roten Blutkörperchen (Erythrozyten) zuständig ist. So kommt es bei CKD-Betroffenen auch zu Entzündungen und Eisenmangel. Bislang erhalten Patient:innen zur Therapie Epo oder andere sogenannte Erythropoese-Stimulatoren (ESA). Doch besonders diejenigen mit fortgeschrittener CKD haben bei diesen Medikamenten ein hohes Risiko für eine Thrombose, einen Herzinfarkt oder Schlaganfall. Beim Therapieerfolg spielen individuelle Faktoren der Patient:innen eine große Rolle.
Ziel: Bessere und personalisierte Behandlung von Anämie
Um die Anämie-Behandlung zu verbessern, entwickeln Forscher:innen beim Projekt NephrESA ein Computermodell, mit dem sich Risiken und Prognosen für die Medikation bei jedem einzelnen Betroffenen ermitteln lassen. Ziel ist es, mit diesem Wissen eine personalisierte und letztlich verbesserte Anämie-Behandlung von Nierenkranken zu ermöglichen. Um die Anwendung und Dosierung Epo-haltiger Arzneimittel zu optimieren und künftig besser individuell auf Patient:innen anpassen zu können, untersuchen die Wissenschaftler:innen, darunter die Arbeitsgruppe Proteomics am ISAS, zunächst die Komplexität der Wechselwirkungen, Entzündungsprozesse, Veränderungen in der Regulation des Eisenstoffwechsels sowie etwa die Thrombosegefahr bei CKD-Betroffenen. Das Wissen soll anschließend in mathematische Modelle einfließen, damit Ärzte zukünftig belastbare und individuell auf Anämie-Patient:innen zugeschnittene Therapievorhersagen treffen können.
Suche nach Markern für frühzeitige Aktivierung der Blutgerinnung
Im Teilprojekt 4 am ISAS geht es um den bislang unerforschten molekularen Mechanismus, der dafür sorgt, dass die Thrombozyten bei CKD-Patient:innen aus dem Gleichgewicht geraten. Die Forscher:innen untersuchen mittels Massenspektrometrie Blutplasma und Thrombozyten von CKD-Patient:innen, um Marker für die frühzeitige Aktivierung der Blutgerinnung zu identifizieren.
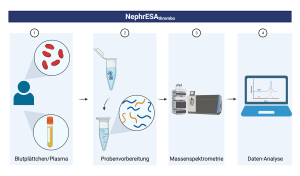
Vom Testsystem bis zum Computermodell: Im Teilprojekt 4 bei NephrESA verfolgen Forschende am ISAS vier Hauptziele.
© ISAS
Zusammenfassung Hauptziele ISAS-Teilprojekt
Entwicklung von Testsystemen (Assays) für Blutplasma-Risikofaktoren für thrombovaskuläre (Blutplättchen und Gefäße betreffende) Ereignisse.
Entwicklung von Assays für den Aktivierungsstatus von Thrombozyten bei CDK-Patient:innen.
Analyse von Veränderungen in der Dynamik der Thrombozyten-Aktivierung bei CKD-Patient:innen.
Entwicklung eines Computermodells (NephrESAthrombo-Submodell) des thrombovaskulären Risikos für CKD-Patient:innen.
Weitere Informationen zu allen Teilprojekten enthält die NephrESA-Projektseite.
Teilen
Ausgewählte Publikationen
International Journal of Molecular Sciences, Bd. 22, Nr. 9, 2021
Shevchuk O, Begonja AJ, Gambaryan S, Totzeck M, Rassaf T, Huber TB, Greinacher A, Renne T, Sickmann A.
Proteomics: A Tool to Study Platelet Function
https://doi.org/10.3390/ijms22094776
